在过去的十年中,增材制造从一种利基制造技术发展成为助听器、金属椎间融合器的首选制造方法。近日,FDA宣布建立医疗器械增材制造实验室,以增强 FDA 处理增材制造产品上市前和上市后问题的准备能力,该实验室被称为 FDA 增材制造实验室,是 CDRH 科学与工程实验室办公室 (OSEL) 的 20 个研究项目之一。
增材制造工艺的测试和验证存在相当大的不确定性,特别是在预测医疗设备的性能方面。这种不确定性阻碍了创新,阻碍了投资,并减缓了增材制造在医疗领域的采用。其次,增材制造涵盖了涉及硬件、软件和材料的广泛技术,所有这些技术都在不断发展。
这种不断的发展需要对工艺验证和监管审查的具体细节进行持续调整,从而带来了额外的挑战。此外,增材制造缩短了供应链,使得椅旁治疗成为可能,这促使临床医生和医院探索其现场制造医疗设备的潜力,这需要监管机构的指导。
2016年5月,美国FDA首次发布3D打印医疗器材指引草案,为应对不断创新且日新月异的3D打印技术发展,美国FDA于2017年12月5日公告了增材制造医疗器材的技术考虑规范。该规范包含设备设计、功能、产品耐久性测试及品质要求等三维打印医疗产品制造技术指导。为确保法规的监管方式适合此种独特且创新技术,该规范的建构基于美国食品和药物管理局对100多项使用3D打印的医疗产品进行审查的经验基础,包含有膝盖置换物、植入物、重建颅骨及第一种通过3D打印生产的癫痫药物,该药物比起传统药物具有多孔基质,可加速药物溶解。
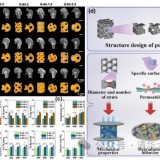
2023年2月,专注于骨科植入物的医疗技术公司Curiteva推出首款获得FDA 510(k)许可的3D打印PEEK颈椎融合器植入物。该植入物设计采用了面向增材制造的多孔设计以及专利的HAFUSE(羟基磷灰石)表面纳米纹理。
2015年2月,MedShape收到FDA对其FastForward骨栓板(Bone Tether Plate)发放的510(k)许可。该骨栓板是MedShape公司FastForward脚趾囊肿校正系统的主要组成部分之一,是MedShape使用医疗级钛合金(TI-6AL-4V)3D打印而成。3D打印技术的应用使得MedShape能够设计出结构复杂、近似现有人体骨骼的产品。
2015年7月,美国牛津性能材料公司(OPM)的一款3D打印聚合物植入物SpineFab获得FDA 认证,该植入物也是获得FDA认证的首个承重的聚合物3D打印植入物。此前已经有两款OsteoFab产品通过了FDA认证进入到临床应用阶段,该公司的专利技术OsteoFab是专门针对3D打印植入物的技术。
2015年8月,FDA批准了Aprecia采用3D打印技术制备的处方药SPRITAM ( 左 乙 拉 西 坦 ,levetiracetam)速溶片上市,用于和其他抗癫痫药物联合治疗成人或儿童患者的癫痫部分性发作、肌阵挛发作,以及原发性全身癫痫发作。
2016年4月,FDA批准了一款3D打印多孔钛颈椎椎间融合系统。该系统由医疗植入物生产商Renovis Surgical Technologies公司生产,商品名称为Tesera™SC。Tesera™SC可用于两种脊柱前凸角度,并可以根据情况变动高度和尺寸,以用于特定的椎间高度修复。Tesera™SC融合系统中的多孔的表面结构,这样可以使骨骼在生长时深入植入物,从而最大限度地提高强度、稳定性和稳固性。
FDA于2016年6月批准了两类3D打印脊柱植入,分别是医疗设备公司K2M 的CASCADIA Cervical(颈椎)植入物和CASCADIA AN Lordotic Oblique(前突斜)植入物。获批的这两种脊柱植入物产品分别针对不同的患者,CASCADIA Cervical颈椎椎间系统作为椎间体融合装置,可以对颈段脊柱提供稳定和支持;而CASCADIA AN Lordotic Oblique前凸斜椎间系统,则为外科医生提供了一系列自动设计的间体用于以经椎间孔腰椎的方法进行斜椎的放置。
2017年,FDA批准了一款3D打印植入物产品,该产品是用于治疗骶髂关节疾病的钛金属植入物,在骶髂关节病(SI)微创手术中植入人体。产品制造商为美国医疗器械公司SI-BONE,该公司表示这是FDA批准的首个骶髂关节3D打印植入物。
2017年7月初,Osseus 的颈椎融合器Gemini-C获得了美国FDA的批准。Gemini-C将用于治疗退行性椎间盘疾病。这是一款由钛金属材料和PEEK 材料制造的脊椎类植入物, 该植入物既具有钛金属植入物所拥有的多孔钛结构,又具有PEEK 植入物所具有的射线透射和生物力学性能。在制造中没有使用注射成型技术,而是使用了3D打印技术。在植入物成型后并未使用常见喷涂技术对植入物进行涂层。
2017年10月初,美国食品和药物管理局(FDA)批准了两款3D打印脊柱植入物。其中一款是有美国脊椎器械制造商ChoiceSpine LP 公司生产的3D打印钛椎体植入物HAWKEYE Ti,另一款是由Nexxt Spine公司生产的NEXXT MATRIXX 3D打印脊柱植入物。
2023年3月,创新脊柱植入系统领先制造商 CoreLink, LLC的Siber® Ti 骶髂关节融合系统获得了FDA的510(k)许可。Siber Ti 系统可提供全多孔纳米表面3D打印植入物产品组合。Siber® Ti 骶髂关节融合系统采用了 CoreLink 的专利 Mimetic Metal® 技术,旨在模拟具有定向晶格结构和小梁孔的天然骨骼,同时具有宏观、微观和纳米(MNM)水平的特征。
… …
迄今为止,FDA-美国食品和药物管理局已批准 100多种使用增材制造技术制造的医疗器械产品。但更广泛的医疗设备界尚未充分实现增材制造。
通过FDA建立增材制造实验室,这使得FDA可以致力于在特定感兴趣领域进行监管科学研究。其中包括与各种先进制造技术类型的工艺验证和工艺监控相关的活动。另一个重点是解决与遵守质量体系法规相关的问题,这需要设计有效的性能测试方法来评估晶格结构并确定优化拓扑的关键参数。
知之既深,行之则远。基于全球范围内精湛的制造业专家智囊网络,3D科学谷为业界提供全球视角的增材与智能制造深度观察。有关增材制造领域的更多分析,请关注3D科学谷发布的白皮书系列。
白皮书下载 l 加入3D科学谷QQ群:106477771
网站投稿 l 发送至2509957133@qq.com
欢迎转载 l 转载请注明来源3D科学谷 l 链接到3D科学谷网站原文